Abstrak
Pengembangan rute sintetis untuk menghasilkan enantiopure ( R )-sitronelal sebagai perantara utama untuk sintesis (–)-mentol dan terpenoid berharga lainnya sangat relevan dalam industri farmasi, rasa, dan wewangian. Di sini, kami memamerkan kaskade dengan dua langkah biokatalitik berturut-turut yang dilakukan secara terpisah menggunakan selektivitas inheren dari dehidrogenase alkohol rantai pendek (SDR) dan reduktase ene (ERED) dari keluarga Old Yellow Enzyme (OYE). Reaksi pertama melibatkan oksidasi geraniol yang relatif murah yang dikatalisis oleh Aa SDR1 dalam sistem bifasik, yang menyediakan geranial sebagai perantara. Fase organik yang mengandung geranial kemudian diekstraksi dan dipindahkan ke langkah kedua, di mana varian ERED OYE2_Y83V mengkatalisis reduksi geranial asimetris untuk menghasilkan ( R )-sitronelal, mencapai >90% konversi dan >99% kelebihan enantiomerik. Penggunaan n -heptana dalam sistem dua fase cairan tidak hanya memfasilitasi pelarutan substrat dan produk tetapi juga meminimalkan isomerisasi geranial. Oleh karena itu, kaskade biokatalitik ini memungkinkan sintesis enantiopure ( R )-sitronelal.
1 Pendahuluan
Citronellal adalah senyawa dengan penggunaan serbaguna, dikenal luas karena aroma lemon, mawar, dan citronella yang khas, sehingga menjadikannya bahan utama dalam perasa dan wewangian. [ 1 ] Khususnya, ( R )-enantiomer dari citronellal adalah zat antara penting dalam sintesis industri (–)-menthol, senyawa kiral, dengan kepentingan komersial yang signifikan dan salah satu perasa yang paling banyak dikonsumsi secara global. 1 , 2 Dari delapan isomer mentol, (–)-menthol memiliki efek pendinginan tertentu dan bau peppermint mint yang diinginkan. 1 , 3 Permintaannya yang meningkat telah mendorong transisi dari ekstraksi alami ke sintesis kimia. Jalur sintesis konvensional melibatkan penggunaan m -kresol, citral, atau mirsen, sebagai bahan awal, dengan zat antara ( R )-citronellal yang umumnya disintesis menggunakan katalis logam dengan ligan kiral seperti kompleks rodium (Skema S1, Informasi Pendukung). [ 4 ]
Meskipun strategi ini menghasilkan konversi yang tinggi, logam beracun dan ligan kiral kompleks yang digunakan dapat menyebabkan pembentukan produk sampingan dan perlunya pemurnian yang ekstensif karena selektivitasnya yang tidak sempurna (≈87% ee ( R )-citronellal untuk proses BASF). [ 4 ] Oleh karena itu, metode alternatif yang lebih berkelanjutan harus diselidiki dan dikembangkan lebih lanjut. [ 5 ]
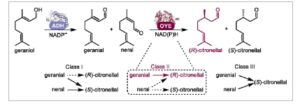
Biokatalisis telah muncul sebagai pendekatan yang menjanjikan untuk mengatasi tantangan ini dengan selektivitas enzim yang sangat baik. [ 6 ] Reaksi enzimatik yang ideal untuk menghasilkan enantiopure ( R )-sitronelal akan melalui reduksi asimetris citral, campuran neral dan geranial ( Gambar 1 ). Dalam hal ini, nikotinamida adenina dinukleotida NAD(P)H-tergantung flavin mononukleotida FMN-mengandung reduktase ena (ERED) dari keluarga enzim kuning tua (OYE, EC 1.6.99.1) telah menunjukkan efisiensinya untuk reduksi asimetris berbagai senyawa α,β-tak jenuh. [ 7 ] Namun, OYE saat ini tidak dapat sepenuhnya mengubah citral menjadi enantiopure ( R )-sitronelal. [ 8 ] Penyaringan berbagai kelas OYE 7 mengungkapkan bahwa kelas I mengubah citral menjadi ( S )-citronellal yang dominan, kelas II umumnya mengubah geranial menjadi ( R )-citronellal dan neral menjadi sebagian besar ( S )-citronellal, sedangkan kelas III biasanya mengubah neral dan geranial menjadi ( S )-citronellal enantiopure (Gambar 1 ). 8
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
Sintesis enzimatik ( R )-sitronelal dari geraniol melalui ADH dan OYE dalam sistem dua fase cair, termasuk reduksi asimetris yang dikatalisis OYE dari sitral menjadi sitronelal menurut kelas I–III. 7
Peningkatan skala dengan OYE2.6 (kelas II, dari Pichia stipitis ) dapat mencapai 67% hasil isolasi ( R )-sitronelal dengan 98% ee , meskipun dari geranial yang baru disiapkan. [ 9 ] Studi mutasi mengungkapkan bahwa selektivitas NCR (kelas I, dari Zymomonas mobilis ) untuk reduksi geranial dapat ditingkatkan dengan NCR mutan ganda W66A_I231A menjadi 63% ee ( R )-sitronelal. 8 Meskipun menjanjikan, upaya rekayasa masih diperlukan untuk OYE kelas I untuk menghasilkan setidaknya >90% ee R . OYE2p yang baru-baru ini dikarakterisasi (kelas II, dari Saccharomyces cerevisiae YJM1341) menghasilkan 87,2% hasil dan 88,8% ee ( R )-sitronelal dari citral. [ 10 ] Setelah mutagenesis, Zheng et al. memperoleh varian tunggal OYE2p_Y84V, yang memungkinkan konversi seluruh sel dari citral menjadi ( R )-sitronelal dengan hingga 95,4% ee . [ 11 ] Menggunakan varian ini yang digabungkan dengan rekayasa alkohol dehidrogenase (ADH), Lin dan rekan mengembangkan kaskade sel utuh in vivo dari 150 mM geraniol dengan 30% v/v heksana, menghasilkan 72,3% ( R )-sitronelal dengan 96,7% ee , masih beberapa persen kurang dari enantiopuritas. [ 12 ] Meskipun penulis bertujuan untuk proses redoks-netral, penambahan 30 mM NADH diperlukan untuk mendapatkan konversi yang lebih tinggi; oleh karena itu, rekayasa lebih lanjut dari kaskade ADH–ERED in vivo ini diperlukan.
Baru-baru ini, kami mengembangkan kaskade satu-pot in vitro menggunakan radikal alkohol oksidase tembaga ( Cgr AlcOx) dan OYE2 (kelas II, dari Saccharomyces cerevisiae S288C) dari geraniol 20 mM menjadi ( R )-sitronelal, mencapai konversi 95,1% dan ee 95,9% . [ 13 ] Salah satu keterbatasannya adalah penghambatan Cgr AlcOx oleh sitronelal dan isomerisasi geranial menjadi neral. Untuk mengatasi tantangan ini, penelitian ini menyajikan kaskade biokatalitik yang menggunakan ADH dari famili dehidrogenase rantai pendek (SDR), khususnya Aa SDR1 dari Aedes aegypti , [ 14 ] untuk mengkatalisis oksidasi geraniol menjadi geranial dalam sistem dua fase cair, dikombinasikan dengan OYE2 untuk menghasilkan ( R )-sitronelal enantiopure (Gambar 1 ). Pendekatan ini memanfaatkan oksidasi geraniol menjadi geranial dalam sistem bifasik pelarut organik-air [ 15 ] dengan meminimalkan isomerisasi geranial menjadi neral yang terjadi dalam media air, sehingga meningkatkan reduksi enantioselektif geranial selanjutnya.
2 Hasil dan Pembahasan
Sebelum menjalankan kaskade enzimatik penuh, efisiensi setiap langkah dievaluasi secara terpisah.
2.1 Oksidasi Geraniol yang Dikatalisis ADH
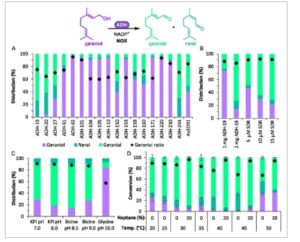
Bahasa Indonesia: Untuk mengidentifikasi enzim yang cocok untuk oksidasi geraniol selektif menjadi geranial, penyaringan 17 ADH dari Johnson Matthey (kit enzim reduksi CO EZK003) bersama dengan Aa SDR1 murni kami (lihat SI) dilakukan, menggunakan NADH-oksidase (NOX) untuk mendaur ulang NAD(P ( Gambar 2A ) . Penyaringan ini mengungkapkan bahwa ADH-19 dan Aa SDR1 memberikan konversi dan rasio geranial:neral yang paling menjanjikan setelah 6 jam reaksi pada 30 °C. Seperti yang diharapkan, peningkatan konsentrasi Aa SDR1 dari 1 menjadi 15 μM dan pengurangan waktu reaksi menjadi 1 jam meningkatkan konversi dan selektivitas terhadap geranial (Gambar 2B ), dengan konversi 78% dan rasio geranial:neral 91:9. Aktivitas spesifik dan konversi Aa SDR1 diukur dalam buffer dan unit pH yang berbeda dari 7,0 hingga 10,0, dengan yang terbaik konversi keseluruhan dan rasio geranial:neral dengan buffer KP i pada pH 8,0 (Gambar 2C , Gambar S3, Informasi Pendukung). Enzim ini stabil dan aktif (1,6–1,8 U mg −1 ) hingga pH 9,0; setelah itu, konversi turun menjadi 26% pada pH 10,0.
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
Oksidasi geraniol yang dikatalisis ADH. A) Penyaringan ADH (CFE dari kit JM dan Aa SDR1). Kondisi: dalam 1 mL, 100 mM buffer KP i pH 8,0, 1 mM NAD(P) + , 2 mg mL −1 NOX CFE, 1 mg mL −1 ADH CFE atau 1 μM Aa SDR1 murni , 10 mM geraniol (dari stok 1 M dalam DMSO, 1% v/v), dan 30 °C, 900 rpm, 6 jam. Berlian hitam menunjukkan rasio geraniol:neral. B) Reaksi ADH-19 dan Aa SDR1 dalam 1 jam. Kondisi yang sama seperti (A) dan 1 jam. C) Pengaruh pH. Kondisi: 50 mM buffer (MOPS-NaOH, KP i , Bicine, Glycine) pada pH 7–10, 25 μM Aa SDR1, kondisi yang sama seperti (A) dan 1 jam. D) Pengaruh suhu dan 20% v/v n -heptana. Kondisi: dalam 1,2 mL, 10 mM geraniol (dari stok 1 M dalam DMSO, 1% v/v), 1 mM NADP + , 25 μM Aa SDR1, 2 mg mL −1 NOX CFE, 0 atau 20% v/v n -heptana, 20–50 °C, 900 rpm, dan 1 jam. Rata-rata duplikat.
Kami juga mengevaluasi pengaruh suhu dan media reaksi pada oksidasi geraniol yang dikatalisis Aa SDR1 (Gambar 2D ). Dalam buffer pada suhu 30 °C, reaksi mencapai konversi 92%, dengan 86:14 geranial:neral setelah 1 jam. Dalam sistem bifasik yang mengandung 20% v/v n -heptana, konversi adalah 95%, dengan rasio geranial:neral 95:5 yang ditingkatkan, yang menunjukkan peran pelarut organik dalam meminimalkan isomerisasi geranial. Meningkatkan suhu dari 30 hingga 40 °C dengan 20% v/v n -heptana meningkatkan konversi keseluruhan menjadi 99%, sambil mempertahankan rasio geranial:neral 95:5. Sebaliknya, dalam buffer, suhu pada dan di atas 40 °C menghasilkan isomerisasi geranial yang lebih tinggi menjadi neral dan penurunan konversi. Suhu yang lebih rendah pada suhu 20 dan 25 °C menghasilkan konversi keseluruhan yang lebih rendah. Oleh karena itu, suhu 40 °C dalam sistem bifasik dengan 20% v/v n -heptana dalam buffer KP i pH 8 dipertahankan untuk reaksi selanjutnya. Studi ini menunjukkan, untuk pertama kalinya, aplikasi dan kesesuaian Aa SDR1 dalam sistem bifasik untuk memaksimalkan konversi dan meminimalkan isomerisasi produk.
2.2 Reduksi Citral yang Dikatalisis OYE
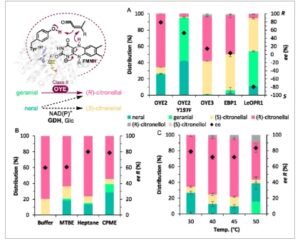
Skrining dengan OYE yang tersedia dari kelas II, OYE2, OYE3, EBP1, dan Le OPR1 dari kelas I dilakukan untuk mengevaluasi efisiensinya dalam mereduksi citral menjadi ( R )-sitronellal dalam waktu 1 jam ( Gambar 3 A ). Selain itu, kami menguji mutan tunggal OYE2_Y197F, karena tirosin 197 diyakini memainkan peran kunci di situs aktif dengan menyumbangkan proton ke substrat karbon -α (Gambar 3 ). [ 16 ] OYE2 wt mencapai 74% konversi dari citral, dengan 78,8% ee ( R )-sitronellal (Gambar 3A , nilai dalam Tabel S2, Informasi Pendukung). Mutasi OYE2_Y197F hanya memberikan 4% konversi, yang dengan jelas menguraikan peran Y197 sebagai donor proton. OYE3 (dari Saccharomyces cerevisiae S288C) dan EBP1 (dari Candida albicans ) memberikan konversi yang hampir penuh pada 99% dan 94%, masing-masing, tetapi dengan nilai ee yang lebih rendah sebesar 14,4% dan 3,3%. Le OPR1 (dari Solanum lycopersicum ) menunjukkan konversi sebesar 57% dan selektivitas yang jelas untuk mengubah neral menjadi ( S )-enantiomer, dengan 79,2% ee , yang sejalan dengan literatur. [ 17 ] Mempertimbangkan bahwa ee tertinggi diperoleh dengan OYE2, kami melakukan profil rangkaian waktu reduksi sitral dalam buffer, yang menunjukkan bahwa geranial direduksi menjadi ( R )-sitronelal lebih cepat daripada neral, dan seiring waktu neral direduksi menjadi ( S )- dan ( R )-sitronelal (Gambar S6A, Informasi Pendukung). Konversi penuh diperoleh dalam 4 jam bersama dengan penurunan signifikan hingga 60% ee ( R )-citronellal, sehingga menyoroti pentingnya menghasilkan geranial murni dari langkah pertama kaskade.
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
A) Penyaringan ERED untuk reduksi asimetris sitral. Kondisi: dalam 1 mL, 50 mM buffer KP i pH 8, 1 mM NADP + , 20 mM glukosa (Glc), 10 U mL −1 Bs GDH, 5 μM OYE, 10 mM sitral (sebagai 1% v/v dalam DMSO), 30 °C, 900 rpm, 1 jam. Rata-rata duplikat. B) Pengaruh pelarut pada 30 °C. Reaksi dalam buffer: 5 μM OYE2, 4 jam. Reaksi dengan pelarut: 7 μM OYE2, pelarut organik 20% MTBE, n -heptana atau CPME, 8 jam. C) Pengaruh suhu. Kondisi: sama seperti (A), 1 jam. Rata-rata duplikat.
Seperti yang disebutkan sebelumnya, geranial diketahui berisomerisasi menjadi neral dalam media penyangga; oleh karena itu, sistem bifasik juga akan menguntungkan langkah OYE untuk memperoleh kemurnian ( R )-sitronelal tertinggi. [ 18 ] Penelitian sebelumnya telah menunjukkan bahwa OYE dapat mempertahankan aktivitas dalam pelarut organik, seperti OYE1 (kelas II, dari Saccharomyces pastorianus ), yang mencapai konversi 90% dalam pelarut organik hingga 97% untuk bioreduksi asimetris substrat alkena labil air. [ 19 ] Demikian pula, Ts OYE (kelas III, dari Thermus scotoductus ) diimobilisasi pada celite untuk mereduksi berbagai alkena dalam metil tert- butil eter (MTBE) dengan air minimal. [ 20 ] OYE3 dan NCR (kelas I, dari Zymomonas mobilis ) juga diimobilisasi dan digunakan dalam pelarut organik hingga 20% v/v. [ 21 ] Oleh karena itu, tiga pelarut organik yang tidak bercampur dengan air, MTBE, n -heptana, dan siklopentil metil eter (CPME), yang biasanya ditoleransi dengan baik dalam sistem bifasik enzimatik, [ 15 ] dievaluasi dan dipilih berdasarkan kompatibilitasnya dengan sistem reaksi dan efisiensi ekstraksi (Gambar 3B ). Dari ketiganya, n -heptana menghasilkan konversi tertinggi sebesar 82% dalam 8 jam. CPME mencapai ee yang sama sebesar 83,3%, tetapi dengan konversi keseluruhan yang rendah sebesar 55%. Pola yang sama diamati ketika fase organik ditingkatkan menjadi 30%, dengan konversi yang lebih rendah di semua pelarut (data tidak ditampilkan). Meskipun MTBE tampaknya memungkinkan kapasitas ekstraksi yang lebih baik, 20% v/v n -heptana memberikan konversi dan ee tertinggi .
Selain itu, pengaruh suhu terhadap konversi juga diteliti, yang menunjukkan pembentukan ( R )-sitronelal yang lebih tinggi pada suhu 45 °C (Gambar 3C ). Namun, suhu >45 °C menghasilkan nilai ee yang lebih rendah karena peningkatan isomerisasi geranial menjadi neral. Berdasarkan temuan ini, suhu 40 °C dipilih untuk percobaan berikutnya.
2.3 Kaskade Penuh: Produksi ( R )-Sitronelal dari Geraniol yang Dikatalisis Aa SDR1-OYE2
Pendekatan awal untuk memproduksi ( R )-sitronelal dari geraniol melibatkan kaskade bienzimatik redoks netral satu pot dalam media yang sepenuhnya berair. Sistem ini terdiri dari dua langkah utama: pertama, oksidasi geraniol menjadi geranial oleh Aa SDR1, dengan NADP + sebagai akseptor hidrida. Selanjutnya, geranial direduksi menjadi ( R )-sitronelal yang dikatalisis oleh OYE2, menggunakan NADPH yang dihasilkan pada langkah pertama, dengan demikian mendaur ulang kofaktor. Namun, selama reaksi enzimatik gabungan, Aa SDR1 tidak hanya mengoksidasi geraniol menjadi sitral tetapi juga mereduksi ( R )-sitronelal menjadi ( R )-sitronelol. Reaksi samping menghasilkan 85,2% ( R )-sitronelal yang diubah menjadi ( R )-sitronelol, dengan demikian secara signifikan mengurangi hasil menuju produk ( R )-sitronelal yang diinginkan. Pengurangan berlebih ini menghadirkan tantangan pada kaskade redoks-netral satu pot, yang membutuhkan pengembangan pendekatan alternatif. Akibatnya, sistem enzimatik bifasik dikembangkan, yang melibatkan dua langkah terpisah yang berurutan untuk mengatasi masalah ini dan meningkatkan efisiensi dan spesifisitas keseluruhan produksi ( R )-sitronelal.
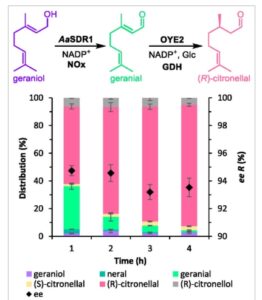
Mengambil kondisi ideal yang ditentukan pada langkah pertama, oksidasi geraniol yang dikatalisis Aa SDR1 dilakukan pada suhu 40 °C dengan 20% v/v n -heptana selama 1 jam, setelah itu geranial diekstraksi dengan n -heptana dan dimasukkan langsung ke langkah kedua dari kaskade. Reduksi geranial yang dikatalisis OYE2 dengan demikian dilakukan dalam sistem bifasik pada suhu 40 °C. Sebuah studi rentang waktu konversi dan nilai ee dilakukan selama periode 4 jam ( Gambar 4 , nilai dalam entri Tabel S3 1–4, Informasi Pendukung). Seperti yang diantisipasi, konversi meningkat seiring waktu, meskipun sedikit penurunan ee diamati dari 95% menjadi 94%, yang disebabkan oleh adanya sejumlah kecil neral yang diubah menjadi ( S )-sitronelal.
Gambar 4
Buka di penampil gambar
Kekuatan Gambar
Kaskade enzimatik Aa SDR1-OYE2 dari geraniol ke ( R )-sitronelal. Kondisi: Langkah pertama: 50 mM KP i pH 8, 2 mg mL −1 CFE NOX, 1 mM NADP + , 25 μM Aa SDR1, 10 mM geraniol (1% v/v DMSO), 200 μL n -heptana, volume akhir 1,2 mL, 40 °C, 900 rpm, 1 jam. Langkah ke-2: 50 mM KP i pH 8, 50 mmol Glc, 1 mmol NADP + , 10 U mL −1 Bs GDH, 10 μmol OYE2 wt, dan 200 μL campuran n -heptana yang mengandung geranial dari langkah pertama, volume akhir 1 mL, 40 °C, 900 rpm. Rata-rata duplikat.
Meskipun ada perbaikan ini, 6–8% ( R )-sitronelol muncul sebagai produk sampingan, yang disebabkan oleh aktivitas Bs GDH yang tidak menentu, yang mereduksi ( R )-sitronelal menjadi ( R )-sitronelol. Untuk mengurangi hal ini, kami bereksperimen dengan memvariasikan jumlah Bs GDH dalam sistem daur ulang kofaktor ( Tabel 1 , entri 1–4). Penurunan jumlah Bs GDH dari 10 menjadi 7 atau 5 U mL −1 menurunkan produksi ( R )-sitronelol menjadi 4%. Sistem daur ulang alternatif menggunakan format atau fosfit dehidrogenase dapat digunakan untuk lebih mencegah reduksi berlebihan menjadi sitronelol ini.
Tabel 1. Kaskade enzimatik Aa SDR1-OYE2 untuk produksi ( R )-sitronelal pada suhu 40 °C. a)
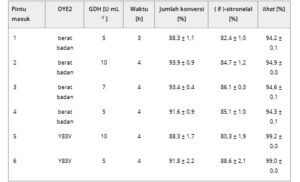
a) Lihat kondisi pada Gambar 4 ; kemurnian geraniol 98%. Total konversi = konsumsi geraniol. Rata-rata duplikat.
Untuk meningkatkan selektivitas langkah kedua, kami menghasilkan mutan OYE2 tunggal Y83V, T38A, dan T38C (Tabel S2, Informasi Pendukung). OYE2_Y83V menghasilkan kinerja keseluruhan terbaik dengan konversi 76% dan ee 94,6% . Mutan T38A dan T38C menunjukkan konversi yang lebih rendah masing-masing sebesar 60% dan 36%, namun nilai ee serupa dibandingkan dengan OYE2 wt (Tabel S2, entri 3–4, Informasi Pendukung).
Secara keseluruhan, mutan OYE2_Y83V membedakan dirinya dengan konversi yang lebih tinggi dan enantioselektivitas yang ditingkatkan, yang sejalan dengan hasil Zheng et al. dengan mutan OYE2p_Y84V (posisi ekuivalen dengan OYE2_Y83V). [ 10 , 11 ] Dari simulasi dinamika dan docking molekuler, Wei dan rekan kerja menunjukkan bahwa mutasi ini memberikan jarak yang lebih pendek untuk transfer hidrida dan proton ke geranial dan neral, meningkatkan efisiensi katalitiknya. [ 11 ] Selain itu, mutasi menginduksi mode pengikatan selektif ( R ) yang dimodifikasi untuk neral, meningkatkan selektivitas. Aktivitas spesifik OYE2 wt dan Y83V diukur untuk citral dan sikloheksenon sebagai substrat patokan ( Tabel 2 ). Mutasi Y83V menunjukkan peningkatan hampir empat kali lipat dalam aktivitas reduksi sitral, dari 0,37 menjadi 1,38 U mg −1 , yang mengonfirmasi konversi lebih tinggi yang diamati, sedangkan aktivitas untuk reduksi sikloheksenon tetap serupa pada 3,23–3,63 U mg −1 .
Tabel 2. Aktivitas spesifik OYE2 yang diperoleh dengan citral dan sikloheksenon.

a) Kondisi: 50 mM buffer KP i pH 8, 0,2 mM NADPH, 10 mM substrat dari stok 1 M dalam DMSO), OYE, pada suhu 40 °C untuk sitral dan pada suhu 25 °C untuk sikloheksenon. Rata-rata duplikat.
Percobaan kaskade penuh berikutnya dengan mutan OYE2_Y83V menunjukkan selektivitas tertinggi untuk memproduksi ( R )-sitronelal, mencapai konversi 88–92% dan 99,2–99,0% ee , dengan sisa geraniol 3,9–7,6% dan 2,8–7,7% ( R )-sitronelol dengan 10 dan 5 U mL −1 Bs GDH, masing-masing (Tabel 1 , entri 5–6). Peningkatan skala 18 mg menghasilkan konversi keseluruhan 88,5%, menghasilkan 77,5% ( R )-sitronelal dengan ee 99,4% (lihat SI untuk detailnya). Ini merupakan ee tertinggi yang dilaporkan untuk ( R )-sitronelal. Kinerja OYE2_Y83V menyoroti potensinya sebagai biokatalis yang efektif, menetapkan standar baru untuk enantioselektivitas dalam biosintesis ( R )-sitronelal. Implementasi lebih lanjut dari varian ini untuk kaskade lain dan peningkatan skala sedang berlangsung.
3 Kesimpulan
Dalam studi ini, kami mengembangkan kaskade enzimatik dengan SDR dan OYE2 yang menghasilkan enantiopure ( R )-sitronelal dari geraniol yang hemat biaya dan tersedia. Desain pendekatan ini dalam sistem bifasik n -heptana-buffer 20% v/v secara efektif meminimalkan isomerisasi yang terkait dengan reduksi citral oleh OYE. Varian OYE2_Y83V secara signifikan meningkatkan selektivitas, mencapai 99,4% ee yang belum pernah terjadi sebelumnya , nilai tertinggi yang dilaporkan untuk produksi ( R )-sitronelal. Kemajuan ini menggarisbawahi potensi metodologi ini sebagai rute sintetis untuk enantiopure ( R )-sitronelal, yang secara langsung dapat berfungsi sebagai perantara utama dalam sintesis (–)-mentol dan terpenoid berharga lainnya. Kombinasi yang sesuai antara Aa SDR1 dan mutan OYE2_Y83V dapat ditingkatkan menjadi proses redoks-netral, melalui rekayasa SDR menuju aktivitas oksidatif yang lebih tinggi, atau melalui imobilisasi [ 22 ] dan dalam sistem aliran, yang telah mendapatkan banyak minat. [ 23 ]
4 Bagian Eksperimen
Keterangan Umum
Bahan kimia diperoleh dari Merck Sigma-Aldrich, TCI Europe, abcr GmbH dan digunakan sebagaimana mestinya. Secara khusus, bahan kimia berikut diperoleh dari Merk Sigma-Aldrich, geraniol (dengan kemurnian >98% dan 90%, CAS 106-24-1), citral (>95%, CAS 5392-40-5), ( R )-(+)-citronellal (CAS 2385-77-5), dan ( S )-(–)-citronellal (CAS 5949-05-3), dan NADPH (CAS 2646-71-1) dibeli dari Oriental Yeast Co. (OYC Europe), dan NADP + (97,6%, CAS 698999-85-8) dari Prozomix Ltd (Inggris).
Enzim OYE2 wt/T38C/T38A/Y83V/Y197F, OYE3, EBP1, Le OPR1, [ 24 ] Aa SDR1, Bs GDH_E170K_Q252L, dan Sm NOX2_V193R_V194H diproduksi secara rekombinan dalam E. coli dan dimurnikan dengan kromatografi afinitas sebagaimana dijelaskan dalam SI. Kit enzim reduksi JM CO EZK003 diterima dengan senang hati dari Johnson Matthey (Cambridge, Inggris). NAD(P)H oksidase komersial (NOx, CAS 77106-92-4) dibeli dari Prozomix Ltd (Inggris).
Konversi biologis
Reaksi biokatalitik dilakukan dalam volume akhir 1 atau 1,2 mL dalam tabung plastik Eppendorf 2 mL yang terkunci rapat. Campuran reaksi dikocok pada 900 rpm dalam Eppendorf ThermoMixer C dengan ThermoTop, pada suhu dan waktu tertentu, dan diinkubasi di atas es selama 2 menit sebelum ekstraksi.
Oksidasi Geraniol yang Dikatalisis ADH
Kondisi untuk JM ADH CFE dan penyaringan Aa SDR1 untuk oksidasi geraniol adalah: dalam 1 mL, 100 mM buffer KP i pH 8,0, 1 mM NAD(P) + , 2 mg mL −1 NOX, 1 mg ADH atau 1 μM Aa SDR1, dan 10 mM geraniol (dari stok 1 M dalam DMSO, 1% v/v), pada 30 °C, 6 jam, diekstraksi dengan 500 μL EtOAc yang mengandung 5 mM dodekana sebagai standar internal, dipusarkan, dan disentrifugasi (14.000 rpm, 7 menit). Lapisan organik dipisahkan, dikeringkan di atas MgSO 4 anhidrat , dan dipindahkan ke botol GC untuk analisis. Sampel yang mengandung tambahan 20% v/v n -heptana dikenakan proses ekstraksi dua langkah. Ekstraksi pertama dilakukan menggunakan n -heptana, diikuti ekstraksi kedua dengan tambahan 125 μL n -heptana.
ERED-Pengurangan Citral yang Dikatalisis
Reduksi sitral yang dikatalisis ERED dilakukan dalam 1 mL, 50 mM buffer KP i pH 8, 20 mM Glc, 1 mM NADP + , 10 U mL −1 Bs GDH, 5 μM ERED, dan 10 mM sitral (dari stok 1 M dalam DMSO, 1% v/v), pada suhu 30 °C, 1 jam. Untuk sistem bifasik, 200 μL n -heptana ditambahkan. Produk reaksi diekstraksi dengan EtOAc yang mengandung 5 mM dodekana, dipusarkan, dan disentrifugasi (3 menit, 14.000 rpm). Lapisan organik dipisahkan, dikeringkan di atas MgSO 4 anhidrat, dan dipindahkan ke vial GC untuk dianalisis.
Reaksi Kaskade Penuh
Kondisi: Langkah ke-1: 50 mM KP i pH 8, 10 mM geraniol (1% v/v DMSO), 2 mg mL −1 CFE NOX, 1 mM NADP + , 25 μM Aa SDR1, dan 200 μL n -heptana, volume akhir 1,2 mL, 40 °C, 900 rpm, 1 jam. Langkah ke-2: 50 mM KP i pH 8, 50 mmol Glc, 1 mmol NADP + , 10 U mL −1 Bs GDH, 10 μmol OYE2 wt, dan campuran n -heptana 200 μL yang mengandung geranial dari langkah pertama, volume akhir 1 mL, 40 °C, 900 rpm. Setelah inkubasi di atas es, produk reaksi diekstraksi dengan n -heptana, dikeringkan di atas MgSO4 anhidrat , dan dipindahkan ke botol GC untuk dianalisis.
Prosedur Analitis
Kromatografi gas dilakukan pada kromatografi gas Shimadzu GC-2010 (perusahaan Shimadzu, Kyoto, Jepang) yang dilengkapi dengan detektor ionisasi nyala dan kolom kiral Hydrodex ß-TBDAc (Macherey-Nagel, Jerman, 50 m × 0,25 mm × 0,25 μm). Produk dikonfirmasi dengan standar referensi dan GC–MS. Konsentrasi produk diperoleh dengan persamaan kurva kalibrasi menggunakan standar internal dalam EtOAc yang digunakan untuk ekstraksi.
